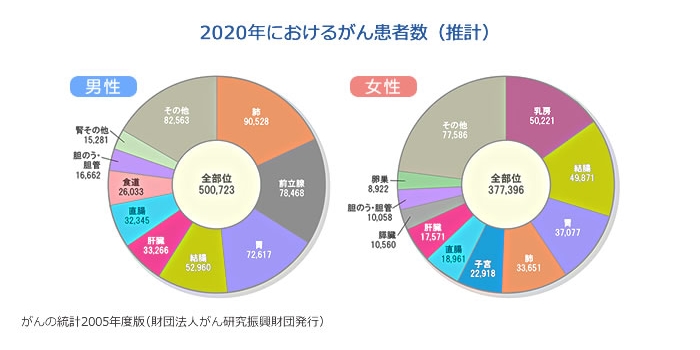
本邦の死因の第1位は悪性新生物となっており、2012年には、360963人(2012年厚生労働省人口動態調査)の方が悪性新生物で亡くなっています。悪性新生物とは、がんやリンパ腫、白血病、肉腫などの悪性腫瘍を一般的に指しますが、その中で肺がんは71518人(1位)であり、これは残念ながら肺がんが治りにくい病気であることを示しています。たばこは吸っても、受動喫煙でも肺がんの危険因子となります!
肺がんの症状とは
咳や血痰等の自覚症状がみられることもありますが、小さな腫瘍や、肺の末梢(肺の隅のほう)にある腫瘍であれば、自覚症状がないこともあります。また肺以外の転移した臓器の痛み、あるいはふらつき、嘔吐などが初発症状であることがあります。
肺の構造
右の図のように、右肺は3つの部分に分かれ、それぞれ上葉(じょうよう)、中葉(ちゅうよう)、下葉(かよう)と呼びます。また左肺は上葉と下葉の2つにわかれています。中心には気管が存在し、左右の主気管支に分岐したのちに、さらに肺の中で細かく枝分かれしていきます。
肺がんの検査
画像検査(胸部単純X線(レントゲン)や胸部CT)で肺がんが疑われた場合、喀痰細胞診、気管支内視鏡検査、エコー(超音波)下生検、CTガイド下肺生検などを行い、細胞や組織を採取して診断をつけますが(顕微鏡でがん細胞がいるか調べます)、場合によっては胸水検査、リンパ節生検(超音波気管支鏡、縦隔鏡など)、局所麻酔下胸腔鏡検査、全身麻酔下に胸腔鏡下肺生検などを行います。また、肺がんと診断したり、肺がんが強く疑われる場合は、転移の有無を調べるための全身の検査として、頭部MRI検査、骨シンチグラフィー、PET検査などを行います。腫瘍マーカー(CEA、シフラ、ProGRP、SLX、SCC、NSE)等を参考にすることもあります。腫瘍マーカーは、それのみでは診断に至りませんが、診断の補助や治療経過観察に使われます。
肺がんの種類
一口に肺がんといっても、顕微鏡検査の結果で数種類の型に分類されます。治療方針を決めるために、下記のように、非小細胞肺がんと小細胞肺がんに分けて考えます。
非小細胞肺がん
扁平上皮がん
男性肺がんの40%程度、女性肺がんの15%程度で喫煙者に多いとされ、発生部位は中心型(肺門型)が多くなっています。
〈特徴〉
- 比較的太い気管支から発生する
- 血痰等の症状が出現する割合が高い
- 喫煙との関係が深い
非扁平上皮がん
扁平上皮がん以外をまとめて分類しています。
-
腺がん
肺がんのなかで最も多く、男性肺がんの40%、女性肺がんの70%を占めます。女性患者の多くは非喫煙者であり、早期では症状がでにくいとされています。
〈特徴〉
- 喫煙との関連は他のタイプに比べて少ない
- 肺の末梢に発生することが多い
- 血痰などの症状が出にくい場合が多い
-
大細胞がん
比較的まれな肺がんで、男性に多いといわれ、進行や転移が早い場合があります。
〈特徴〉
- ほかに分類できないものが混入するため、均一なカテゴリーとは言いにくい面がある
小細胞肺がん
男性・喫煙者に多いタイプで、下記のような特徴があります。小細胞肺がんは小さながん細胞の集団に見えます。
〈特徴〉
- 原発性肺がんのおよそ20%を占める
- 進行が非常に速く、悪性度が高い
- 放射線や抗がん剤に対する感受性が高い
肺がん進行度(病期分類)
肺がんの治療方法を決めるために、がんの大きさや広がり(T因子)、リンパ節への転移(N因子)やその他の臓器への転移(M因子)の状況を示す指標で、TNM分類と呼ばれています。これらの組み合わせで病期(病気の進行度)を決定します。
このように診断のための検査と、全身の状態を評価した検査を組み合わせて、現状を詳細に把握し、適切な治療が受けられるように標準化しているのです。
※スマートフォンの場合はスクロールしてご覧ください
| 潜伏癌 |
TX |
N0 |
M0 |
| 0期 |
Tis |
N0 |
M0 |
| ⅠA期 |
T1mi,a,b,c |
N0 |
M0 |
| ⅠB期 |
T2a |
N0 |
M0 |
| ⅡA期 |
T2a |
N0 |
M0 |
| ⅡB期 |
T1a,b,c |
N1 |
M0 |
| T2a,b |
N1 |
M0 |
| T3 |
N0 |
M0 |
| ⅢA期 |
T1a,b,c |
N2 |
M0 |
| T2a,b |
N2 |
M0 |
| T3 |
N1 |
M0 |
| T4 |
N0,1 |
M0 |
| Ⅲ B期 |
T1a,b,c |
N3 |
M0 |
| T2a,b |
N3 |
M0 |
| T3,4 |
N2 |
M0 |
| Ⅲ C期 |
T3,4 |
N3 |
M0 |
| ⅣA |
Any T |
Any N |
M1a,b |
| ⅣB |
Any T |
Any N |
M1c |
肺がんの治療
小細胞肺がん
-
限局型小細胞がん(LD:limited disease)
根治的放射線照射可能な範囲内に腫瘍や転移のあるリンパ節が含まれている状態で、具体的には、病側の肺門・縦隔リンパ節、そして両側の鎖骨上窩リンパ節までの転移に限られている状態です。
〈治療方法〉
限局型小細胞肺がんでは、対側の肺門リンパ節転移や大量の胸水を認めるものは除きます(同側の胸郭内に加えて、対側縦隔・鎖骨上窩リンパ節までに限る範囲)。限局型小細胞肺がんのうち、ステージⅠ期では標準手術療法を行い、術後に抗がん剤治療(化学療法)を行います。ⅡA期以降の治療は化学療法と放射線治療の組み合わせになります。治療後に完全寛解(病変が画像等で確認できなくなること)が得られた場合は、脳への転移を防ぐために、予防的全脳照射(脳への放射線治療)を行うことがあります。
-
進展型小細胞がん(ED:extensive disease)
LDを超えた範囲に腫瘍が広がっている状態で、胸水や心嚢水に関しての明確な定義はありませんが、大量に胸水が貯留している場合はEDとする場合が多いです。
〈治療方法〉
進展型小細胞肺がんでは、主な治療方法は化学療法となります。
非小細胞肺がん
非小細胞肺がんの治療方針は、ⅠA〜ⅡB期では、肺機能が保たれていて、手術に耐えられる場合には根治術として手術療法を行います。再発予防を目的とした術後補助化学療法として、ⅠA期の一部とⅠB期ではテガフール・ウラシル配合剤(UFT®)を1~2年内服し、ⅡA期以降では点滴による抗がん剤を用いて術後の再発予防を行います。ⅢA期に関しては手術療法、化学療法、放射線治療を組み合わせて治療を行います。ⅢB期では内科的治療が中心となり、化学療法と放射線治療を組み合わせて治療を行います。Ⅳ期では全身状態が保たれていることが前提ですが、主に化学療法が中心となります。適応がある患者さんには、分子標的薬を用います。抗がん剤にはそれぞれ副作用がありますが、新しい制吐薬やステロイドホルモン等を使用することで、以前と比較し、かなり軽減できるようになってきました。
また、肺がんの種類にかかわらず、疼痛などの自覚症状が強い場合は、早期から症状を軽減する治療(緩和治療)を行うことが望ましく、WHOのがん疼痛治療指針をもとに、医療用麻薬や鎮痛補助薬を使用します。骨転移がある患者さんには骨関連事象(病的骨折等)の発現を軽減したり、遅らせたりするためにゾレドレロン酸(ゾメタ®)の点滴やデノスマブ(ランマーク®)の皮下注射を行います。
手術療法について
日本における肺がんに対する手術治療の成績は、1989年には5年生存率が47.8%でしたが、2004年には69.6%まで向上しています。また、手術による周術期の死亡率は0.4%程度と欧米に比較して非常に少ない割合となっています。肺がんに対する手術療法は、現在の医療水準では安全で効果的な治療として肺がん治療の中心を担っています。
術前検査で手術適応を慎重に判断して手術療法が選択されます。非小細胞肺がんⅠA〜ⅡB期の標準治療は肺葉切除+リンパ節郭清となります。病巣のある1つ以上の肺葉を切除し、周囲のリンパ節の摘出(郭清)を行います。当科では、通常の肺がん手術には
胸腔鏡下手術(video-assisted thoracic surgery:VATS)を積極的に行っています。また、進行期肺がんでは、手術適応を慎重に評価し、二葉切除や肺全摘術、他臓器合併切除・再建術などの
拡大手術を、本院心臓血管外科をはじめとする専門家と協力して行っており、さらに根治度を上げる目的で、術前導入・術後補助化学療法や放射線治療も行っております。肺機能の温存を考慮して、小型肺がんや多発肺がんでは
区域切除術(肺葉切除術よりさらに少ない範囲を切除)、部分切除術を行っております。また気道へ浸潤している場合は、
気管・気管支形成術を伴った肺切除を行っております。
化学療法(抗がん剤治療)について
小細胞肺がんや進行期の非小細胞肺がんの治療の中心は化学療法です。当科では、最新のエビデンス(臨床試験等で効果があることが示された証拠や結果)に基づき、肺がんの遺伝子検索(EGFR遺伝子変異やEML4-ALK融合遺伝子など)を積極的に行い、新しい分子標的薬や新規抗がん剤を用いて治療を行っています。
小細胞肺がんの化学療法
限局型では抗がん剤はシスプラチン+エトポシド(PE療法)を3〜4週間毎に4〜6コース行います。進展型ではPE療法のほかにシスプラチン+イリノテカン(PI療法)が行われ、腎機能や副作用等の全身状態に応じてシスプラチンの分割投与やカルボプラチンへの変更を行います。一次治療後に再発した場合は、イリノテカン、ノギテカン、アムルビシン、エトポシド等を中心に化学療法を試みます。
非小細胞肺がんの化学療法
肺がん診療ガイドラインに従い、分子標的薬であるゲフィチニブ(イレッサ®)、エルロチニブ(タルセバ®)、クリゾチニブ(ザーコリ®)、アファチニブ(ジオトリフ®)、ベバシズマブ(アバスチン®)や殺細胞性の抗がん剤であるプラチナ製剤(シスプラチン、ネダプラチン、カルボプラチン)と新規抗がん剤(ペメトレキセド、ドセタキセル、パクリタキセル、ゲムシタビン、ビノレルビン、イリノテカン、TS-1®)など)を用いて、単剤または2剤併用の化学療法を行っています。分子標的薬治療は1日1~2錠の内服治療が基本となり、副作用などに応じて減量したり、隔日投与を行います。点滴抗がん剤は3〜4週毎に4〜6コース繰り返します。初回点滴治療の効果が認められる患者さんには対しては、維持療法(ペメトレキセドやベバシズマブ)を継続して行うことで効果を維持しています。
手術後の患者さんに対しても、ⅠA期の一部と、ⅠB期においてはUFT®を術後1〜2年間内服し、Ⅱ期以降では術後補助化学療法を行い良好な成績をおさめています。また、標準的な術後補助化学療法(シスプラチン+ナベルビン)と比べて、副作用を抑えつつ、効果も同等と考えられるネダプラチン+ドセタキセルによる化学療法や、再発した場合にはカルボプラチン+ナブパクリタキセル(アブラキサン®)による化学療法といった臨床試験を行っております。いずれも3〜4週ごとに4コースを目標として行います。
放射線療法について
本院放射線科の治療専門医と連携し、治療を行います。直線加速器(リニアック)から発生する高エネルギーX線を用い、体の外から照射します。全身状態により手術が困難な患者さんにおける、早期の非小細胞肺がんに対しての呼吸同期下定位放射線治療や、進行がんでは化学療法と組み合わせて治療効果を高める化学放射線療法、骨転移や脳転移に対しての照射、特に脳転移に対しては大きさや個数から判断し、全脳照射や定位放射線治療(Xナイフ)を行います。肺がんに対する根治照射では、1日1回2Gyを週5日の頻度で合計60~66Gy(約6週間)を、肺門・縦隔に照射します。
いずれも治療前にCT画像等を用いてシミュレーションし、最適な治療計画を立てています。他、多発骨転移に対し、疼痛緩和治療であるストロンチウム89(メタストロン®)の内用療法も行っています。
緩和治療について
肺がんは、手術、抗がん剤、放射線治療を組み合わせ、治療を行います。しかし、転移が認められたり、治療にかかわらず増大したりすることがあります。それにより、痛みをはじめとするいろいろな症状、心のつらさなどが出現することがあります。そのような場合に治療と並行し緩和ケアが行われます。
当院では医師(主治医、精神科医)、看護師、薬剤師などで緩和ケアチームを作り、より良い状態でがんと付き合っていけるように、サポートを行います。以前は緩和ケアというと、治療の手立てがなくなったときに行うようなイメージがあったかもしれませんが、最近では緩和ケアによる生存期間の延長が報告されたこともあり、治療開始後、早い時期から積極的に行うことが重要と考えられています。
その他の治療について
既存の標準治療が困難となった患者さんを対象に、腫瘍内科と協力してがんペプチドワクチンを用いた治療も行っております。